Case Reports in Hematology
Volume 2019, Article ID 9651207, 3 pages
https://doi.org/10.1155/2019/9651207
Primary Cutaneous Anaplastic Large Cell Lymphoma of the Oral Cavity Successfully Treated with Brentuximab Vedotin
Department of Biomedicine and Prevention, Haematology Division, University of Tor Vergata, Viale Oxford 81, Rome, Italy
Correspondence should be addressed to Federico Meconi; federico.meconi89@gmail.com
Received 15 April 2019; Revised 20 August 2019; Accepted 5 September 2019; Published 17 September 2019
Academic Editor: Sergio Storti
Copyright © 2019 Federico Meconi et al. This is an open access article distributed under the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Primary cutaneous anaplastic large cell lymphoma is a CD-30 positive lymphoproliferative disorder with good prognosis, usually treated with radiation therapy and surgery. Head, neck, and extremities are the most frequently involved sites. In this paper, we describe an unusual case of oral localization, recurring after skin-involving radiotherapy, successfully treated with sixteen cycles of brentuximab vedotin. This could be a more effective approach with a less detrimental toll for treating these rare disorders.
1. Introduction
Primary cutaneous CD-30 positive lymphoproliferative disorders are a rare and heterogeneous group of primary skin tumors, accounting for about 30% of all cases of primary cutaneous T-cell lymphomas (PCTCL) [1]. The group comprises primary cutaneous anaplastic large cell lymphoma (PCALCL), lymphomatoid papulosis (LyP), and borderline cases.
PCALCL is most commonly found in adults (median age at diagnosis is 60 years old), occurring more often in men than women (3 : 1). Macroscopically, PCALCL usually presents itself with red to violaceous lesions, rapidly growing and frequently ulcerative. Head, neck, and extremities are the most frequently involved sites, both for solitary lesions or for multiple grouped nodules. Systemic symptoms, such as fever, fatigue, and mucosal involvement, are rare in PCALCL. However, in at least 10% of cases, neoplastic CD30+ cells can be found in locoregional lymph nodes. Its course is generally indolent (dissemination is uncommon); spontaneous regression occurs in about 40% of cases, even though partial remission is documented more frequently than complete ones [2–4].
The first line treatment currently accepted is radiation therapy or surgical removal, whenever possible. In case of multifocal lesions, methotrexate is accepted followed by low-dose maintenance [1]. However, brentuximab vedotin (BV) was recently included in the National Comprehensive Cancer Network Guidelines as a first line treatment. Recurrences are common in both the same or in different cutaneous sites. PCALCL carries a favorable prognosis with a 5-year survival rate over 90% [5].
Histopathologically and microscopically, PCALCL exhibits a high expression rate of CD30+ antigen (CD30 positivity is required for diagnosis in at least 75% of atypical cells), positivity for CD4+ antigen and does not present ALK positivity [6]. In this article, we describe a rare case of PCALCL of the hard palate that was successfully treated with BV.
2. Case Report
In November 2016, a 40-year-old Caucasian male came to our attention for a nodular, erythematous, nonulcerated, well-defined, and indurated lesion localized in his right forearm.
A skin punch biopsy of the lesion was performed, showing an inflammatory multinodular infiltration of lymphohistiocytic cells in both deep and superficial dermis, including many large, atypical, anaplastic cells with frequent mitosis, characterized by the following immunohistochemistry: CD45+, CD2+, CD3+/–, CD7+/–, CD20–, CD30+, and ALK–. To rule out systemic anaplastic large cell lymphoma, we performed a bone marrow biopsy (negative for malignant cells) and a CT/PET scan that revealed a significant and singular uptake of 18F-FDG in the right forearm region (matching precisely the tumor localization). As we made diagnosis of PCALCL, the patient began radiation therapy (dose of 3600 cGy), achieving complete response.
A new nodular erythematous lesion of 1 cm appeared in March 2017 in the right inguinal region and was unsuccessfully treated with topical steroids. One month later, when it expanded up to 3 cm, a new CT/PET scan was performed and revealed the lesion as the only pathological uptake in the right inguinal region. The patient underwent another radiation therapy of 3600 cGy, obtaining complete response again.
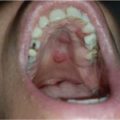
In May 2017, two more nodular lesions appeared in the patient’s oral cavity, in the left hard palate (Figure 1). A punch biopsy showed histopathological and immunohistochemical findings consistent with PCALCL. As the lesions did not show spontaneous regression in one month of clinical observation and the patient was experiencing oral discomfort in eating and chewing, it was decided to proceed with treatment.
Figure 1: Oral cavity before therapy with BV.
3. Conclusions
To the best of our knowledge, this is the first documented case of PCALCL present only in the hard palate, while other few cases of similar processes involving mucosal sites of the head and neck have been previously reported with one case of systemic anaplastic large cell lymphoma involving the hard palate [9].
We demonstrated that oral PCALCL could be successfully treated with systemic immune-chemotherapy with brentuximab vedotin, an anti-CD30 antibody conjugated to monomethyl auristatin E and an effective antimicrotubule agent that was previously approved for Hodgkin lymphoma, ALK-positive anaplastic large cell lymphoma [10], and other cutaneous lymphoproliferative disorders, such as mycosis fungoides.
Using immune-chemotherapy instead of radiation therapy can prevent several side effects, such as mucositis, candidosis, dysgeusia, radiation caries, osteoradionecrosis, soft tissue necrosis, progressive periodontal attachment loss, trismus, and xerostomia, which are all well documented while treating mucosal lesions with radiations [11].
Brentuximab’s most common side effect is peripheral sensitive neuropathy that can lead to dose reduction or even drug withdrawal. However, our patient did not experience such neuropathy and could complete therapy within the sixteen cycles at full dose.
Due to the rarity of this group of cutaneous lymphoproliferative disorders (even rarer if we consider those found in the oral cavity), it is still a challenge to make a trial comparing radiation therapy with immune-chemotherapy using BV. From this case, we can infer that although BV is not side-effect free, it offers a safe choice to treat primary cutaneous CD-30 positive lymphoproliferative disorders no longer responding to radiation therapy and standard chemotherapy or cases where the anatomic site involved does not allow RT or must be avoided due to its side effects.
Conflicts of Interest
The authors declare that there are no conflicts of interest regarding the publication of this paper.
References
- R. C. Melchers, R. Willemze, M. W. Bekkenk et al., “Evaluation of treatment results in multifocal primary cutaneous anaplastic large cell lymphoma: report of the Dutch Cutaneous Lymphoma Group,” British Journal of Dermatology, vol. 179, no. 3, pp. 724–731, 2018.View at Publisher · View at Google Scholar · View at Scopus
- R. Willemze, L. Cerroni, W. Kempf et al., “The 2018 update of the WHO-EORTC classification for primary cutaneous lymphomas,” Blood, vol. 133, no. 16, pp. 1703–1714, 2019.View at Publisher · View at Google Scholar
- D. Gilson, S. J. Whittaker, F. J. Child et al., “British Association of Dermatologists and U.K. Cutaneous Lymphoma Group guidelines for the management of primary cutaneous lymphomas 2018,” British Journal of Dermatology, vol. 180, no. 3, pp. 496–526, 2019.View at Publisher · View at Google Scholar · View at Scopus
- W. Kempf, K. Pfaltz, M. H. Vermeer et al., “EORTC, ISCL, and USCLC consensus recommendations for the treatment of primary cutaneous CD30-positive lymphoproliferative disorders: lymphomatoid papulosis and primary cutaneous anaplastic large-cell lymphoma,” Blood, vol. 118, no. 15, pp. 4024–4035, 2011.View at Publisher · View at Google Scholar · View at Scopus
- M. W. Bekkenk, F. A. Geelen, P. C. van Voorst Vader et al., “Primary and secondary cutaneous CD30(+) lymphoproliferative disorders: a report from the Dutch Cutaneous Lymphoma Group on the long-term follow-up data of 219 patients and guidelines for diagnosis and treatment,” Blood, vol. 95, no. 12, pp. 3653–3661, 2000.View at Google Scholar
- R. Willemze, E. S. Jaffe, G. Burg et al., “WHO-EORTC classification for cutaneous lymphomas,” Blood, vol. 105, no. 10, pp. 3768–3785, 2005.View at Publisher · View at Google Scholar · View at Scopus
- R. Stranzenbach, E. Dippel, M. Schlaak, and R. Stadler, “Brentuximab vedotin in CD30+ cutaneous lymphoma: how do we treat, how shall we treat? A review of the literature,” British Journal of Dermatology, vol. 177, no. 6, pp. 1503–1509, 2017.View at Publisher · View at Google Scholar · View at Scopus
- R. Dummer, Y. H. Kim, S. M. Horwitz et al., “Brentuximab vedotin or physician’s choice in CD30-positive cutaneous T-cell lymphoma (ALCANZA): an international, open-label, randomised, phase 3, multicentre trial,” The Lancet, vol. 390, no. 10094, pp. 555–566, 2017.View at Publisher · View at Google Scholar · View at Scopus
- A. P. Sciallis, M. E. Law, D. J. Inwards et al., “Mucosal CD30-positive T-cell lymphoproliferations of the head and neck show a clinicopathologic spectrum similar to cutaneous CD30-positive T-cell lymphoproliferative disorders,” Modern Pathology, vol. 25, no. 7, pp. 983–992, 2012.View at Publisher · View at Google Scholar · View at Scopus
- P. L. Zinzani, S. Sasse, J. Radford, O. Shonukan, and V. Bonthapally, “Experience of brentuximab vedotin in relapsed/refractory Hodgkin lymphoma and relapsed/refractory systemic anaplastic large-cell lymphoma in the named patient program: review of the literature,” Critical Reviews in Oncology/Hematology, vol. 95, no. 3, pp. 359–369, 2015.View at Publisher · View at Google Scholar · View at Scopus
- E. de Souza Tolentino, B. S. Centurion, L. H. C. Ferreira, A. P. de Souza, J. H. Damante, and I. R. F. Rubira-Bullen, “Oral adverse effects of head and neck radiotherapy: literature review and suggestion of a clinical oral care guideline for irradiated patients,” Journal of Applied Oral Science, vol. 19, no. 5, pp. 448–454, 2011.View at Publisher · View at Google Scholar · View at Scopus
Linfoma Primitivo Cutaneo Anaplastico a Grandi Cellule del cavo orale trattato con successo con Brentuximab Vedotin
Federico Meconi, Roberto Secchi, Raffaele Palmieri, Sara Vaccarini, Vito Mario Rapisarda, Laura Giannì, Fabiana Esposito, Ida Provenzano, Daniela Nasso, Livio Pupo, and Maria Cantonetti
Dipartimento di Biomedicina e Prevenzione, Unità Operativa di Ematologia, Università di Tor Vergata, Viale Oxford 81, Roma, Italia
Recevuto il 15 Aprile 2019; Revisionato il 20 Agosto 2019; Accettato il 5 Settembre 2019; Pubblicato il 17 Settembre 2019
Editore Accademico: Sergio Storti
Il linfoma anaplastico cutaneo primitivo a grandi cellule è un disturbo linfoproliferativo CD-30 positivo con buona prognosi, generalmente trattato con radioterapia e chirurgia. Testa, collo ed estremità sono i siti più frequentemente coinvolti. In questo articolo, descriviamo un insolito caso di localizzazione orale, recidivato dopo radioterapia su precdente coinvolgimento cutaneo, trattata con successo con sedici cicli di brentuximab vedotin. Questo potrebbe essere un approccio più efficace e meno dannoso per il trattamento di questi rari disturbi.
- Introduzione
I disturbi linfoproliferativi positivi CD-30 primitivi cutanei sono un gruppo raro ed eterogeneo di tumori cutanei primitivi, che rappresentano circa il 30% di tutti i casi di linfoma cutaneo primitivo a cellule T (PCTCL) [1]. Il gruppo comprende il linfoma primitivo cutaneo anaplastico a grandi cellule (PCALCL), la papulosi linfomatoide (LyP) e i casi borderline.Il PCALCL si trova più comunemente negli adulti (l’età media alla diagnosi è di 60 anni), più frequente negli uomini rispetto alle donne (3: 1). Macroscopicamente, il PCALCL di solito si presenta con lesioni da rosse a violacee, in rapida crescita e spesso ulcerative.Testa, collo ed estremità sono i siti più frequentemente coinvolti, sia per lesioni solitarie che per noduli multipli raggruppati. Sintomi sistemici, come febbre, affaticamento e coinvolgimento della mucosa, sono rari nel PCALCL. Tuttavia, in almeno il 10% dei casi, le cellule neoplastiche CD30 + possono essere trovate nei linfonodi locoregionali.Il suo corso è generalmente indolente (la diffusione è rara); la regressione spontanea si verifica in circa il 40% dei casi, anche se la remissione parziale è documentata più frequentemente rispetto a quella completa [2-4].
Il trattamento di prima linea attualmente accettato è la radioterapia o la rimozione chirurgica, quando possibile. In caso di lesioni multifocali, viene accettato il metotrexato seguito da un mantenimento a basse dosi.
Tuttavia, brentuximab vedotin (BV) è stato recentemente incluso nelle Linee guida NCCN come trattamento di prima linea. Le recidive sono comuni sia nello stesso sito che diversi siti cutanei. Il PCALCL ha una prognosi favorevole con un tasso di sopravvivenza a 5 anni superiore al 90% [5].
Istopatologicamente e microscopicamente, il PCALCL mostra un alto tasso di espressione dell’antigene CD30 + (la positività CD30 è richiesta per la diagnosi in almeno il 75% delle cellule atipiche), la positività per l’antigene CD4 + e non presenta positività ALK [6]. In questo articolo, descriviamo un raro caso di PCALCL del palato duro che è stato trattato con successo con BV.
- Case Report
Nel novembre 2016, un uomo caucasico di 40 anni è venuto alla nostra attenzione per una lesione nodulare, eritematosa, non ulcerata, ben definita e indurita localizzata nel suo avambraccio destro. È stata eseguita una biopsia cutanea della lesione, che mostrava un’infiltrazione infiammatoria multinodulare di cellule linfoistiocitiche sia nel derma profondo che superficiale, comprese molte cellule grandi, atipiche, anaplastiche con frequente mitosi, caratterizzate dalla seguente immunoistochimica: CD45 +, CD2 +, CD3 +/– , CD7 +/–, CD20–, CD30 + e ALK–. Per escludere il linfoma anaplastico sistemico a grandi cellule, abbiamo eseguito una biopsia del midollo osseo (negativa per cellule maligne) e una TC/PET che ha rivelato un assorbimento significativo e singolare di 18F-FDG nella regione dell’avambraccio destro (corrispondente esattamente alla localizzazione del tumore). Per la diagnosi di PCALCL, il paziente ha iniziato la radioterapia (dose di 3600 cGy), ottenendo una risposta completa. Una nuova lesione eritematosa nodulare di 1 cm è apparsa a Marzo 2017 nella regione inguinale destra ed è stata trattata senza successo con steroidi topici. Un mese dopo, essendo cresciuta fino a 3 cm, fu eseguita una nuova scansione TC/PET e rivelò la lesione come unico assorbimento patologico nella regione inguinale destra. Il paziente ha subito un’altra radioterapia di 3600 cGy, ottenendo di nuovo una risposta completa.
Nel maggio 2017, altre due lesioni nodulari sono comparse nella cavità orale del paziente, nel palato duro sinistro (Figura 1). Una biopsia ha mostrato risultati istopatologici e immunoistochimici coerenti con PCALCL. Poiché le lesioni non hanno mostrato regressione spontanea in un mese di osservazione clinica e il paziente ha avuto disagio orale nel mangiare e nella masticazione, si è deciso di procedere con il trattamento.
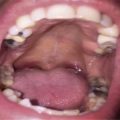
Per evitare la radioterapia e i suoi effetti collaterali e tenendo conto del breve tempo di ricaduta che il paziente aveva sperimentato con una precedente radioterapia in diversi siti, si è deciso di iniziare l’immunochemioterapia sistemica con brentuximab vedotin (BV) 1,8 mg / Kg ogni 21 giorni. Interessanti studi sulla riduzione delle dosi e del numero di cicli di BV sono state pubblicate di recente [7], dimostrando che questi protocolli potrebbero essere efficaci quanto la terapia standard. Dopo solo due cicli di BV, il paziente ha mostrato una regressione completa delle lesioni nodulari con ricomparsa della normale mucosa del cavo orale (Figura 2). La rivalutazione con TC/PET finale è risultata negativa per qualsiasi localizzazione della malattia.
Figura 2: cavità orale dopo il 2o ciclo di BV.
Poiché il paziente non ha presentato alcuna neuropatia e ha avuto una ricaduta precoce dopo la remissione iniziale ottenuta con la radioterapia, abbiamo continuato il trattamento con BV per sedici cicli [8] senza riduzione della dose. Tutti e sedici i cicli sono stati eseguiti poiché non siamo riusciti a trovare alcun dato che dimostri che la riduzione dei cicli potrebbe portare alla stessa sopravvivenza libera da malattia, cercando di garantire al nostro paziente la remissione completa più lunga possibile.
- Conclusioni
Per quanto ne sappiamo, questo è il primo caso documentato di PCALCL presente solo nel palato duro, mentre altri pochi casi di processi simili che coinvolgono siti della testa e del collo sono stati precedentemente segnalati con un caso di linfoma anaplastico sistemico a grandi cellule coinvolgendo il palato duro [9]. Abbiamo dimostrato che il PCALCL orale può essere trattato con successo con l’immunochemioterapia con brentuximab vedotin, un anticorpo anti-CD30 coniugato con monometil auristatina E, un agente antimicrotubulo efficace, precedentemente approvato per il linfoma di Hodgkin, linfoma anaplastico positivo ALK [10 ] e altri disturbi linfoproliferativi cutanei, come la micosi fungoide. L’uso dell’immunoterapia al posto della radioterapia può prevenire diversi effetti collaterali, come mucosite, candidosi, disgeusia, carie radiante, osteoradionecrosi, necrosi dei tessuti molli, perdita progressiva di attacco parodontale, trisma e xerostomia, che sono tutti ben documentati nel trattamento delle lesioni della mucosa con radiazioni [11]. L’effetto indesiderato più comune di Brentuximab è la neuropatia sensitiva periferica che può portare alla riduzione della dose o persino alla sospensione del farmaco. Tuttavia, il nostro paziente non ha manifestato tale neuropatia e ha potuto completare la terapia con i sedici cicli a dose piena. A causa della rarità di questo gruppo di disturbi linfoproliferativi cutanei (ancora più rari se si considerano quelli riscontrati nella cavità orale), è ancora una sfida eseguire uno studio comparativo della radioterapia con l’immunoterapia che utilizza BV. Da questo caso, possiamo dedurre che sebbene il BV non sia privo di effetti collaterali, offre una scelta sicura per il trattamento dei disturbi linfoproliferativi positivi CD-30 cutanei primitivi che non rispondono più alla radioterapia e alla chemioterapia standard o ai casi in cui il sito anatomico coinvolto non consente la RT o deve essere evitato a causa dei suoi effetti collaterali.
“La gratitudine di tutti noi giunga a tutti i soci tramite la tua persona”.
Dott. Federico Meconi